22 . 01 . 2021
A Relação entre a Microbiota Vaginal e as Infecções Urinárias
As infecções do tracto urinário (ITU) são bastante comuns no sexo feminino. Ao invés de um mecanismo linear de infecção, parece existir uma determinante influência da microbiota no processo que exploraremos neste artigo.
Antes do uso disseminado de técnicas de amplificação genética e caracterização de microorganismos, a microbiologia assentava exclusivamente na identificação de agentes infecciosos por visualização directa ou cultura. No caso específico das ITU, a presença de sintomas associada ao isolamento de bactérias patogénicas no exame cultural, permite fazer o diagnóstico e escolher o antibiótico indicado, de acordo com o antibiograma. Este tem sido o paradigma da Infecciologia, que tem salvo muitas vidas, e não deve, de todo, ser descartado.
Contudo, à medida que aprendemos mais sobre as bactérias que habitam o nosso corpo, percebemos que a vasta maioria delas “trabalham” em nosso favor (relação de simbiose). Daí todo o entusiasmo com a investigação científica em torno da microbiota. O principal reservatório de bactérias no organismo está presente no intestino, mas outros locais como os pulmões, orofaringe e vagina, são também importantes, tendo particularidades distintas. A tendência futura da medicina será promover o equilíbrio dos diferentes ecossistemas no corpo, em vez de recorrer apenas ao uso de antibióticos para eliminar os agentes patogénicos. Isto porque, como veremos, os agentes simbióticos têm capacidade de tornar o terreno menos favorável para as espécies patogénicas.
Quão frequentes são as ITU?
A bexiga é um dos locais mais frequentes de infecção no corpo humano, especialmente na mulher, por razões anatómicas. Entre 50-60% das mulheres adultas tem, pelo menos, uma ITU durante a vida (1). Cerca de 1% da população mundial do sexo feminino (70 milhões de mulheres), sofrem mais de seis ITU por ano, o que condiciona a sua qualidade de vida de forma significativa e obriga ao uso recorrente de antibióticos.
Qual é a causa de ITU na mulher?
A teoria prevalente assenta na colonização do intróito (orifício) vaginal por bactérias da flora fecal (Escherichia coli, Klebsiella pneumoniae, etc.). Seguidamente, estas bactérias podem ascender através da uretra, atingindo a bexiga. As mulheres têm uma uretra muito mais curta, o que torna esta deslocação mais fácil. Na maioria das vezes a infecção cinge-se à bexiga, contudo poderá ser mais complicada se ascender ao rim (pielonefrite).
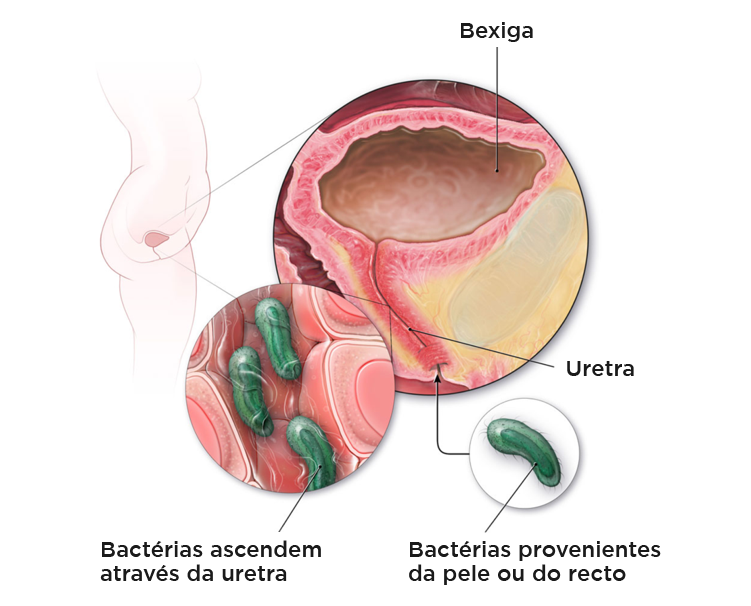
Fig.1 – A colonização e posterior infecção da bexiga, na mulher.
Recentemente, a microbiota urinária também tem sido alvo de estudo e descobriu-se que a urina não é estéril, mesmo na ausência de infecção. Parece haver então um convergência de diversos tipos de microbiota – intestinal, vaginal e urinária – na bexiga, condicionando o possível desenvolvimento de infecções. (2)
O que sabemos acerca da microbiota vaginal?
Ao contrário da microbiota intestinal, em que a diversidade de bactérias é sinal de um ecossistema saudável, na vagina a situação é diferente. Assim, um ecossistema vaginal saudável é composto por mais de 90% de bactérias pertencentes ao género Lactobacillus. Dentro do género, a espécie Lactobacillus crispatus é a mais benéfica. Quanto maior for a diversidade de bactérias na vagina, maior a tendência para o desequilíbrio e aparecimento de infecções várias. (3, 4). Este é o caso da vaginose bacteriana, em que há uma diminuição de Lactobacillus, e aumento da população de Gardnerella vaginalis e outras bactérias anaeróbias (não sobrevivem na presença de oxigénio).
Qual a função dos Lactobacillus na prevenção de ITU?
Os Lactobacillus promovem um ambiente vaginal saudável e diminuição das infecções urinárias, através dos seguintes mecanismos: (5)
- Produção de ácido láctico, o que torna o pH vaginal mais ácido e menos favorável para bactérias patogénicas, como a Escherichia coli.
- Aderência ao epitélio da vagina, competindo assim com os possíveis agentes patogénicos.
- Síntese directa de substâncias com actividade antimicrobiana, como as bacteriocinas.
- Produção de peróxido de hidrogénio (o termo químico para a vulgar água oxigenada) que ajuda na eliminação directa de agentes invasores.
Porque aumenta a frequência de ITU após a menopausa?
Após a menopausa, os níveis de estrogénio diminuem consideravelmente, o que condiciona alterações no ambiente vaginal:
- Atrofia do epitélio.
- Diminuição da população de Lactobacillus.
- Aumento do pH vaginal (devido à menor produção de ácido láctico).
- Aumento da colonização com Enterobacteriaceas (E. coli e outras).
Esta associação ficou patente num estudo que incluiu 463 mulheres em fase de pós-menopausa. Neste estudo, verificou-se que as mulheres que haviam recebido terapêutica hormonal de substituição (com estrogénio) nos últimos 12 meses, tinham níveis de Lactobacillus mais elevados e, inversamente, menor colonização vaginal com Escherichia coli. (6)
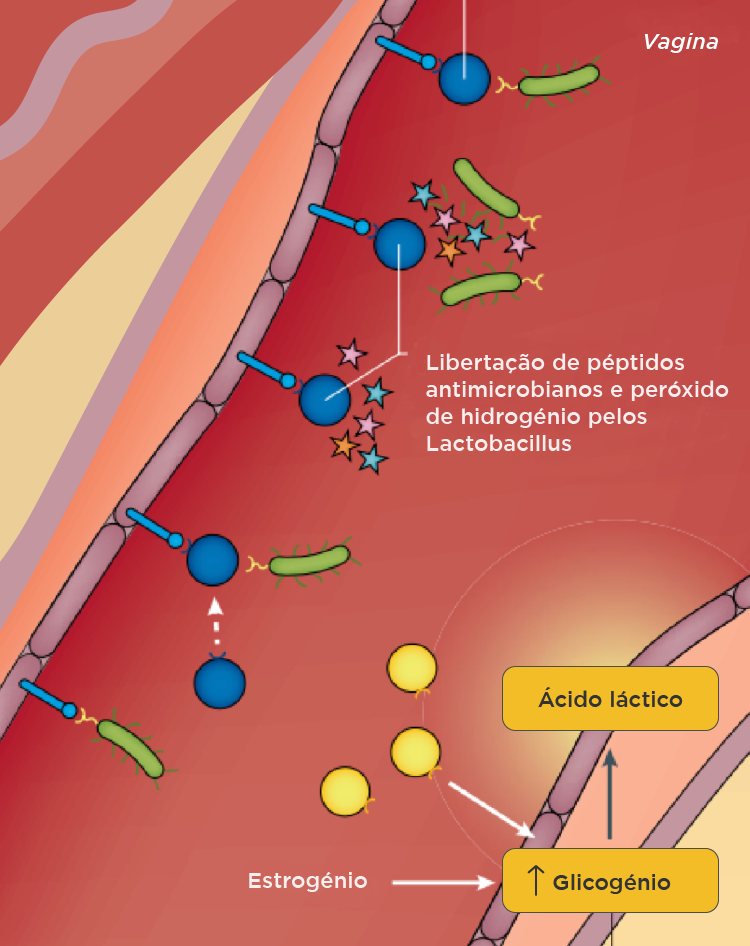
Fig. 2 – O estrogénio aumenta as reservas de glicogénio no epitélio vaginal. Os Lactobacillus produzem ácido láctico, a partir do glicogénio, e acidificam o pH, além de também produzirem substâncias com actividade antimicrobiana directa (7).
Que alternativas de tratamento existem?
O uso de antibióticos é muitas vezes necessário para controlar a ITU. Contudo, o uso recorrente de antibióticos promove o aparecimento de estirpes bacterianas resistentes e danifica o equilíbrio da microbiota a nível intestinal, e não só. Está documentado o aumento da frequência de ITU em mulheres após a toma de antibióticos (8). Podemos, então, perceber como muitas mulheres caem num círculo vicioso de infecções urinárias e toma de antibióticos.
Como medidas alternativas ou complementares para restabelecer o equilíbrio da microbiota, podemos enumerar as seguintes:
- Optimização da microbiota intestinal, através de uma dieta diversificada, rica em polifenóis e fibra. Lembremo-nos que o reservatório das bactérias que provocam ITU está no intestino.
- Uso de probióticos por via oral e/ou vaginal (9, 10).
- Administração intra-vaginal de prebióticos, como a lactulose, para estimular a proliferação de Lactobacillus (11).
- Uso de D-manose, um açúcar simples, que previne a ligação de certas bactérias, como a E. coli, ao epitélio da bexiga (7).
- Tratamento de mulheres em idade pós menopausa com estrogénio tópico ou terapêutica hormonal de substituição (caso não haja contra-indicação). (6)
As ITU, especialmente quando recorrentes, são mais complexas do que se possa inicialmente pensar. Uma abordagem integrativa, que vise restabelecer o equilíbrio entre a paciente e a sua flora, terá maior probabilidade de sucesso. Aliás, esta será, seguramente, a resposta para muitas das doenças com que vivemos.
Referências:
1. Medina, M., & Castillo-Pino, E. (2019). An introduction to the epidemiology and burden of urinary tract infections. Therapeutic advances in urology, 11, 1756287219832172.
2. Meštrović T, Matijašić M, Perić M, Čipčić Paljetak H, Barešić A, Verbanac D. The Role of Gut, Vaginal, and Urinary Microbiome in Urinary Tract Infections: From Bench to Bedside. Diagnostics. 2021; 11(1):7.
3. Stapleton AE. The Vaginal Microbiota and Urinary Tract Infection. Microbiol Spectr. 2016 Dec;4(6):10.1128/microbiolspec.UTI-0025-2016.
4. van de Wijgert JH, Borgdorff H, Verhelst R, et al. The vaginal microbiota: what have we learned after a decade of molecular characterization?. PLoS One. 2014;9(8):e105998.
5. Butler DSC, Silvestroni A, Stapleton AE. Cytoprotective Effect of Lactobacillus crispatus CTV-05 against Uropathogenic E. coli. Pathogens. 2016;5(1):27.
6. Wendy L. Pabich, Stephan D. Fihn, Walter E. Stamm, Delia Scholes, Edward J. Boyko, Kalpana Gupta, Prevalence and Determinants of Vaginal Flora Alterations in Postmenopausal Women. The Journal of Infectious Diseases, Volume 188, Issue 7, 1 October 2003, Pages 1054–1058,
7. Sihra, N., Goodman, A., Zakri, R. et al. Nonantibiotic prevention and management of recurrent urinary tract infection. Nat Rev Urol 15, 750–776 (2018).
8. Smith HS, Hughes JP, Hooton TM, Roberts P, Scholes D, Stergachis A, Stapleton A, Stamm WE. Antecedent antimicrobial use increases the risk of uncomplicated cystitis in young women. Clin Infect Dis. 1997 Jul;25(1):63-8.
9. Koradia P, Kapadia S, Trivedi Y, Chanchu G, Harper A. Probiotic and cranberry supplementation for preventing recurrent uncomplicated urinary tract infections in premenopausal women: a controlled pilot study. Expert Rev Anti Infect Ther. 2019 Sep;17(9):733-740.
10. Stapleton AE, Au-Yeung M, Hooton TM, Fredricks DN, Roberts PL, Czaja CA, Yarova-Yarovaya Y, Fiedler T, Cox M, Stamm WE. Randomized, placebo-controlled phase 2 trial of a Lactobacillus crispatus probiotic given intravaginally for prevention of recurrent urinary tract infection. Clin Infect Dis. 2011 May;52(10):1212-7.
11. Collins SL, McMillan A, Seney S, van der Veer C, Kort R, Sumarah MW, Reid G. Promising Prebiotic Candidate Established by Evaluation of Lactitol, Lactulose, Raffinose, and Oligofructose for Maintenance of a Lactobacillus-Dominated Vaginal Microbiota. Appl Environ Microbiol. 2018 Feb 14;84(5):e02200-17.
Gostei
Obrigado.
Uma explicação fabulosa.Esta é a medicina que eu aprecio.Obrigada doutor
Obrigado pelo interesse!